Parveen K. Garg a, Robyn L. McClelland b, Nancy S. Jenny c, Michael H. Criqui d, Philip Greenland e, f, Robert S. Rosenson g, David S. Siscovick h, Neal Jorgensen b, Mary Cushman c, i, *
a Division of Cardiovascular Medicine, Keck School of Medicine, University of Southern California, Los Angeles, CA, USA
b Department of Biostatistics, University of Washington, Seattle, WA, USA
c Department of Pathology and Laboratory Medicine, University of Vermont College of Medicine, Burlington, VT, USA
d Department of Family & Preventive Medicine, University of California in San Diego, La Jolla, CA, USA
e Department of Medicine, Feinberg School of Medicine, Northwestern University, Chicago, IL, USA
f Department of Preventive Medicine, Feinberg School of Medicine, Northwestern University, Chicago, IL, USA
g Mount Sinai Heart, Icahn School of Medicine at Mount Sinai, New York, NY, USA
h New York Academy of Medicine, New York, NY, USA
i Department of Medicine, University of Vermont College of Medicine, Burlington, VT, USA
摘要
目的:多项前瞻性研究指出脂蛋白相关磷脂酶A2(Lp-PLA2)质量和活性与突发心血管疾病呈正相关,但研究对象主要为白人。本研究评估了多种族健康群体中Lp-PLA2与首发心血管疾病事件(CVD)的相关性,并在入选时对受试者有无亚临床动脉粥样硬化进行确认。
方法:基线时检测5456位参与此项多种族动脉粥样硬化研究的受试者的Lp-PLA2质量和活性水平。评估受试者基线时有无亚临床疾病(冠脉钙化分数>0或颈动脉内膜-中层厚度>第80百分位)并随访可能发生的CVD事件(冠心病、缺血性卒中、心血管疾病导致的死亡)。
结果:随访10.2年(中位数),516例患者发生了突发性CVD事件。在校正过的Cox比例-风险模型中,Lp-PLA2质量和活性的标准差升高均与心血管事件风险升高相关:Lp-PLA2活性的风险比(HR:95%置信区间(CI)为1.12(1.01-1.26),Lp-PLA2质量的风险比为1.10(1.01-1.21)。该相关性不受亚临床症状疾病状态的影响(Lp-PLA2活性交互作用的P值为0.99,质量交互作用的P值为0.32)且亚临床动脉粥样硬化的检测结果对其也无混杂作用。对于中国受试者,Lp-PLA2活性而不是质量有较弱的关联性,但是中国受试者的心血管事件相对较少。
结论:对于多种族人群,Lp-PLA2与CVD风险正相关,与是否存在冠脉钙化或者颈动脉内膜中层增厚无关。
1.引言
脂蛋白相关磷脂酶A2(Lp-PLA2)为50kDa的非钙离子依赖的酶类,粥样硬化损伤时在巨噬细胞中高表达[1,2]。Lp-PLA2能水解LDL微粒中的氧化磷脂[3,4]。斑块中Lp-PLA2的出现和发挥活性可能与易损、破溃的斑块有关[5]。因此,Lp-PLA2可能成为血管炎症的特异性标志物。
以往对于无普遍心血管疾病(CVD)的个体研表明较高的Lp-PLA2质量和活性升高与突发的冠心病、缺血性卒中相关[7-12]。这些研究的对象主要为白人,即使是非白种人也主要是亚洲人群。此外,以往的研究并未评估亚临床脉粥样硬化对心血管疾病风险与Lp-PLA2相关性的影响。有亚临床动脉粥样硬化的群体较无亚临床动脉粥样硬化的患者发生CVD的风险为高[13]。如果与无亚临床疾病的个体相比,有亚临床疾病的个体的Lp-PLA2与发生CVD的相关性更高,或能确定出通过口服Lp-PLA2抑制剂减少原发性心血管疾病的人群。然而在稳定冠心病(CHD)患者中,口服Lp-PLA2抑制剂虽然降低了冠脉事件的风险,却没有显著减少复合结局中心血管疾病导致的死亡、心肌梗死(MI)或卒中的发生[14]。
我们评估了多种族健康人群Lp-PLA2与突发心血管事件的关系并在基线时评估受试者是否有亚临床动脉粥样硬化。我们假设有亚临床动脉粥样硬化的受试者的Lp-PLA2与心血管事件的关联更强。
2.材料和方法
2.1动脉粥样硬化多种族研究(MESA)群体
2000年7月至2002年9月,MESA从6个中心城市(巴尔的摩,马里兰州;芝加哥,伊利诺斯州;福赛斯县,北卡罗莱纳州;洛杉矶,加利福利亚州;纽约,纽约州及圣保罗,明尼苏达州)招募了6814名成年受试者(45-84岁),并进行基线检测[15]。该研究的受试者包括白人(38%),美国黑人(28%),西班牙人(22%)及美籍华人(12%)且均无已知的临床CVD。2002至2007年,MESA对受试者进行了3项后续检查。每个地区的制度评审委员会均认可该研究并且所有受试者均签订了知情同意书。
2.2危险因素评估
入选时,通过标准化的调查问卷获得人口统计学信息、受教育水平、家庭年收入、吸烟史以及高血压、高血脂、高胆固醇或糖尿病的药物治疗史。吸烟用“包•年”计算,并且分为:正在抽烟,曾经抽烟和不抽烟三种。身体质量指数(BMI)计算方法为体重(公斤)/身高(米)的平方。测得受试者坐位时的心脏收缩压和舒张压[16]。
2.3血清测量
禁食十二小时后采血,检测总胆固醇、高密度胆固醇、甘油三酯和葡糖糖水平。使用Firedwald方程计算低密度脂蛋白胆固醇。空腹葡萄糖含量>125mg/dl或使用降血糖药定义为糖尿病患者。使用高灵敏度的分析方法检测C-反应蛋白(CRP)(N-高敏CRP;德灵公司,迪尔菲尔德,伊利诺伊州;批间变异系数:2.1-5.7%)。
2.4血浆Lp-PLA2测量
基线检查时检测血浆中Lp-PLA2质量和活性。样品送diaDexus有限公司(南旧金山,加利福利亚洲)进行检测[17]。Lp-PLA2质量的检测采用双抗体夹心-酶联免疫吸附法(PLACTM测试;diaDexus)。Lp-PLA2活性由以氚标记的血小板活化因子(PFA)类似物为底物的酶学试验测定。Lp-PLA2质量和活性的批间变异系数分别为6.0%及5.0%。1328名受试者的Lp-PLA2结果不可用,原因是该研究未取得其中一个商业实体的同意。
2.5亚临床动脉粥样硬化的检测
扫描中心使用心电门控电子束CT或多层螺旋CT系统评估冠脉钙化程度(CAC)[18]。连续两次对受试者和已知体内钙浓度的体模进行扫描。体模包含4条含有已知的钙密度的线条,用以校正不同机器测量时X射线的衰减。放射科医师或心脏病医师在中央阅读中心(Harbor-UCLA医疗中心/洛杉矶生物研究中心,托伦斯,加利福利亚)完成所有CT扫描结果的阅读工作。CAC值大于零定义为异常。所有分析均采用经体模校正的钙化评分的平均值[19]。
颈动脉内膜中层厚度(CIMT)的超声检测结果在塔夫茨大学-新英格兰医学中心,波士顿,马萨诸塞州进行解读,参照以前文献[20]报道的方法。左右两侧颈内动脉(ICA)及颈总动脉(CCA)的近端、远端壁IMT的平均最大值定义为最大IMT值。CIMT值达到ICA或CCA最高值的五分之一即界定为异常。
2.6随访
每隔9-12个月,联系受试者或其家庭成员就是否有以下事件进行随访:短期入院治疗,门诊诊断为CVD以及死亡。随访持续到2011年。专业人员从医院记录中提取数据以核实自述报告的调查信息。若受试者在医院外发生心血管死亡事件则联系其近亲和医师。MESA死亡发病率复合委员会的两位医生成员独立对事件进行分类。若有分歧,由全体委员最后分类。
事件分为由CVD引起的或CHD引起的。CVD事件包括非致命心肌梗死(MI)、心脏骤停后复苏、CVD死亡、血管重建相关的明确或可能的心绞痛以及缺血性卒中。CHD事件包括非致命心肌梗死,心脏骤停后复苏,CHD死亡,血管重建相关的明确或可能的心绞痛。其中有一部分CHD事件定义为严重的CHD事件,包括CHD死亡或非致命心肌梗死。CVD终点不包括未在心绞痛诊断之前进行的血管重建术。MI的诊断依赖于临床症状、心电图表现及外周血中心脏标记物的水平。如果死亡发生在心肌梗死后28天内,或者死亡前72小时内有胸痛,或者有CHD史并且无已知的非动脉粥样硬化、非心脏的死因,则认为死亡与CHD有关。审核人将通过心肺复苏术(包括复率法)从完全心脏骤停成功恢复的情况归类为心脏骤停复苏。评审员根据自己的临床判断对心绞痛进行分级。对确定或可能的心绞痛的分级需要清晰、明确的症状(不同于诊断心肌梗死)描述。确定的心绞痛的分类还需要可逆性心肌缺血或阻塞性冠状动脉疾病的客观证据。MESA随访方法的更多细节描述见http://www.Mesanhlbi.org/followup.aspx。
2.7统计分析
比较发生与未发生CVD事件患者的基线特征,连续变量采用t检验,分类变量采用卡方检验。
基线时Lp-PLA2质量和活性标准差增加与伴随的心血管事件间的联系可采用经年龄、性别、种族/族裔、体重指数(BMI)、糖尿病、吸烟状况、收缩压、总胆固醇和高密度脂蛋白胆固醇、他汀类药物使用、抗高血压药使用、受教育水平、CRP、无临床症状动脉粥样硬化的连续测定(最大CCA IMT,最大ICA IMT,和CAC)校正后的Cox比例风险模型评估。由于受试者可能处在Lp-PLA2升高发展为CVD的阶段,故模型需同时在校正和不校正亚临床疾病度量的情况下运行。使用ln(CAC+1)转换对数据进行分析。在以下各个心血管终点进行上述分析:(1)CVD,(2)CHD,及(3)CHD(严重)。使用广义相加模型确定结果是否显著违反线性假设。似乎所有的联系都可以很好地由线性模型代表。对Lp-PLA2变量与年龄、性别、种族/族裔、无临床症状的CVD进行相乘交互作用检测。交互作用P值小于0.05则具有统计学意义上的显著性。分层结果按种族/族裔以及有无亚临床动脉粥样硬化显示。
3.结果
5486(80.5%)名MESA受试者基线时检测了Lp-PLA2质量和活性,30例由于没有随访数据而排除。缺少Lp-PLA2检测数据的中国人较少而黑人较多。除此以外,进行Lp-PLA2检测或未进行检测的受试者的基线特征无有意义的差异。
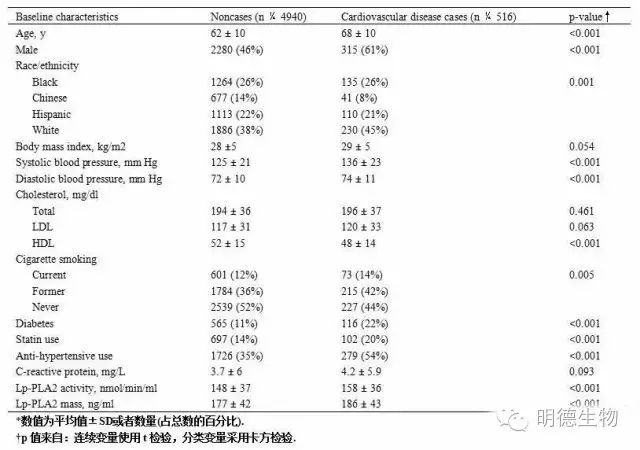
随访中发生了516例明确的心血管事件,358例由CHD引起,其中223例为“严重”事件。研究人群的基线特征见表1。与未发生事件的受试者相比,发生CVD事件的受试者年龄更大且为多为男性。他们的血液收缩压和舒张压明显更高,高密度脂蛋白水平明显更低。在发生CVD事件的患者中,糖尿病,他汀类药物及抗高血压药的使用更加普遍。与不抽烟的人相比,现在或者曾经抽烟的人发生CVD的比例更高。与未发生事件的受试者相比,发生CVD事件,CHD事件和严重CHD事件的受试者Lp-PLA2质量和活性水平都更高(表2)。
表1 研究受试者的基线描述*.
(可点击放大查看)
经年龄、性别、种族/族裔、体重指数(BMI)、糖尿病、吸烟状况、收缩压、总胆固醇和高密度脂蛋白胆固醇、他汀类药物及抗高血压药使用、受教育水平、CRP校正的Cox比例风险模型中,Lp-PLA2质量和活性都与CVD,CHD及“严重”CHD风险的增加有关,且与“严重”CHD风险增加的相关性最大(表3)。增加亚临床动脉粥样硬化连续测量结果(最大CCA IMT ,最大ICA IMT和CAC)的校正后,Lp-PLA2质量和活性与CVD、CHD及“严重”CHD发生的风险比几乎完全相同。
表2 随后病发状态的Lp-PLA2平均质量和活性(n 5456)*.
(可点击放大查看)
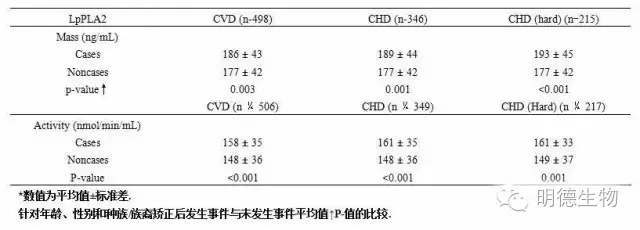
对年龄、性别和种族/族裔校正后,基线时进行他汀类药物治疗的受试者群体(n=879)Lp-PLA2质量的升高与CVD(HR 1.06,95%CI 0.87-1.29)、CHD(HR1.14,95%CI 0.91-1.41)及“严重”CHD(HR 1.24,95%CI 0.93-1.64)风险的增加无关。同样,Lp-PLA2活性的升高也与CVD(HR 1.12,95%CI 0.89-1.41)、CHD(HR1.24,95%CI 0.96-1.60)及“严重”CHD(HR 1.39,95%CI 0.99-1.97)风险的增加无关。
表3 Lp-PLA2水平与心血管疾病事件风险的联系(n5456).
(可点击放大查看)

检验Lp-PLA2与性别的交互作用时发现Lp-PLA2质量与CHD(pinteraction=0.01)及“严重”CHD终点(p interaction=0.02)具有显著交互作用。与女性相比,男性Lp-PLA2与CHD事件的相关性更强。Lp-PLA2活性和性别与CHD、“严重”CHD的交互作用项分别为0.19和0.12。对于CVD终点,Lp-PLA2质量和活性无论与CRP还是性别都没有显著交互性。
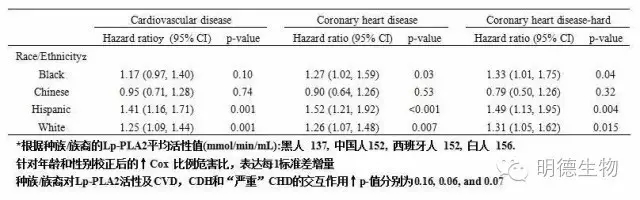
有证据证明经种族/族裔对Lp-PLA2活性于CVD(交互作用p=0.16),CHD(p 交互作用=0.06)和“严重”CHD(交互作用p=0.07)终点的交互作用存在修饰效应,但仍未未达到我们严格的显著性水平。在对年龄和性别的校正分析中,中国人Lp-PLA2活性升高与CVD事件(HR0.95,95%CI 0.71-1.28)、CHD事件(HR0.90,95%CI 0.64-1.26)或“严重”CHD事件(HR0.79,95%CI 0.50-1.26)风险的增加无关。参与的中国人中CVD,CHD和“严重”CHD事件发生的数量分别是41、32和17。黑人Lp-PLA2活性升高与CVD事件关系的显著性接近临界线(p=0.10),在黑人、西班牙人和白人中Lp-PLA2活性升高与三个重点事件的所有其他联系都具有显著性且结果类似(表4)。
表4 由种族/族裔分层的Lp-PLA2活性与心血管事件发生的风险的联系*.
(可点击放大查看)
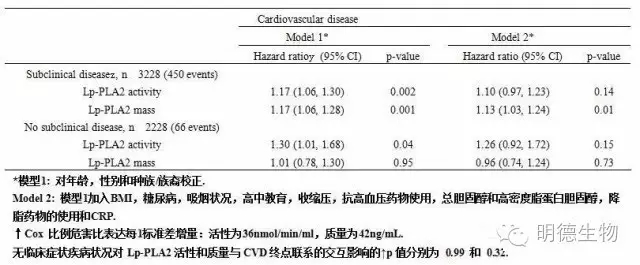
有证据证实3228位受试者患有亚临床疾病,其中450人经历了心血管事件。经年龄、性别和总胆固醇校正后,Lp-PLA2质量和活性与颈动脉IMT或CAC都没有显著相关性。对于基线时有亚临床疾病的个体,无论是Lp-PLA2质量还是活性均与CVD事件风险的增加相关(表5)。在2228名基线证实无亚临床疾病的受试者中,只有66名发生了心血管事件。Lp-PLA2活性而非质量与CVD事件风险的增加有关。尽管有或无亚临床疾病的患者Lp-PLA2质量与CVD的相关性有明显的区别,但Lp-PLA2质量与亚临床疾病的交互作用项无统计学显著性(p=0.32,在校正了年龄,性别和种族/族裔后的模型中)
表5 Lp-PLA2与根据无临床症状疾病分层的心血管疾病事件发生的风险的联系(n 5456)
(可点击放大查看)
4.讨论
在基线时无临床CVD的多种族群体中,Lp-PLA2质量和活性的升高均与与CVD和CHD发生率的增加有关。无论受试者基线时有无亚临床疾病(即是否存在钙化冠脉疾病或颈动脉内膜中层增厚),Lp-PLA2活性的升高均与CVD风险的增加相关。尽管有亚临床疾病的受试者,而不是无亚临床疾病的患者Lp-PLA2质量升高与CVD风险升高相关,但这种亚临床疾病状态引起的差异并无无统计学意义。
以往有研究报道白人和亚洲人Lp-PLA2水平升高与CVD风险增加存在相关性。本研究得到的风险比与以往的研究一致[8-10,12,21-24]。最近发表的一项包含32项前瞻性研究的荟萃分析中,突发冠心病及缺血性卒中与Lp-PLA2质量每标准差的增加的相关性分别是1.11和1.14,而与Lp-PLA2活性每标准差的增加的相关性分别是1.10和1.08[7]。然而在这项荟萃分析中,Lp-PLA2活性与无血管疾病史的患者的冠心病事件无关。这与我们的研究结果不同[7]。
以往的研究较少以多种族人群为研究对象,而此项研究结果将此前的发现延伸到了多种族群体中。不同种族中心血管事件的风险会随Lp-PLA2质量和活性的升高而增加,而中国人心血管事件的风险与Lp-PLA2活性无关。中国人某一基因多态性的高流行性也许与这些发现有关。PLA2G7的V279F等位基因的突变就与Lp-PLA2活性降低有关[25,26]。这些基因多态性在亚洲人中发生的频率更高,日本人中为25%,中国人和韩国人中大于10%[27-29]。韩国男性的横断面研究发现,基因多态性的出现与CAD患病率减少20%有关[30]。然而,在一项关于中国人群的研究中,这一多态性与缺血性卒中的风险无关[31]。在两项包含高加索人种的大型荟萃分析中,未证实CVD事件风险降低与基因多态性之间存在联系[29,32]。本研究在中国人中未发现相关性也许是由于事件数量本身较少或是偶然的原因。
检测Lp-PLA2可以检测其质量也可以检测其活性。以往有研究同时检测了Lp-PLA2的质量和活性,但两种测量方法的相关性仅为中等[22]。活性可能更能反映Lp-PLA2诱导的炎症状态[22]。而最近的一项荟萃分析指出,无论测量Lp-PLA2的活性还是质量,其风险率是相似的,即对于心血管预后,两种检测方法表现相似,这与我们的结果一致[7]。虽然本研究结果表明性别校正对Lp-PLA2质量与CHD的联系有影响,但这些发现都可能是由于偶然性,因为同样的荟萃分析并未显示性别对Lp-PLA2质量与CHD的相关性有影响[7]。
与未使用他汀类药物的患者相比,在基线时使用他汀类药物的患者中发生过心血管事件的患者的比例更高。基线时使用他汀类药物治疗的受试者群体中,Lp-PLA2质量和活性与心血管疾病事件的风险比虽然没有统计学显著性,但与其在整个群体中的关联性是相似的。缺少显著性可能是由于能力有限,而且Lp-PLA2水平可能是一个与基线时是否使用他汀类药物无关的风险因子。
由于Lp-PLA2被认为是一种血管炎症标记物,我们假设与无亚临床动脉粥样硬化的受试者相比,基线时有亚临床动脉粥样硬化的患者的Lp-PLA2水平对CVD事件预测价值更大,然而在研究中未发现此现象。然而,一项心血管健康研究的报道中指出,仅在使用颈动脉超声检测到动脉粥样硬化的患者中CRP水平升高与CVD风险有关[33]。
我们的研究中Lp-PLA2质量和活性都与颈动脉IMT和CAC具有弱相关性。而关于Lp-PLA2与亚临床动脉粥样硬化度量的相关性的研究给出的结果也不一致。心血管健康研究和马尔默饮食与癌症研究都指出Lp-PLA2活性升高与颈动脉IMT升高之间存在相关性[34,35]。而其他研究则指出Lp-PLA2活性与颈动脉粥样硬化之间没有相关性[36,37]。而对于CAC,在年轻人中冠状动脉风险的发展的研究中,经包括LDL和HDL胆固醇在内的心血管风险因子进行校正后,Lp-PLA2质量而非活性的升高与冠状动脉斑块的出现和严重程度相关[39,40]。
本研究指出Lp-PLA2与CVD事件似乎是通过某项与这里评价的亚临床症状无关的机制相互关联的。在一项对冠脉钙化分数为0的病人的研究中,CT冠状动脉造影证实其中11%的患者有非钙化斑块[41]。此前一项研究证实Lp-PLA2的降低可减少坏死核心体积但并未减少冠状动脉粥样硬化斑块中总的粥样化体积[42]。我们的发现表明Lp-PLA2可识别出与亚临床疾病传统度量无关的易损斑块。因此,Lp-PLA2可能有助于识别出心血管事件的高风险人群,且无需考虑是否存在可测量的亚临床动脉粥样硬化。
我们的研究也有不足之处。受试人群收入了基线时无已知临床CVD的患者,并且结果不能被推广到与本研究不同的群体中。在分层分析中,一些阶层的CVD事件的数量太低。根据亚临床疾病或某些种族进行分层时,Lp-PLA2与心血管疾病事件之间缺少相关性,原因可能是模型的分析能力较差。为进一步研究这些问题,需要进行其他研究或者更长时间的随访。不应排除非缺血性心脏病,因为它也是心脏骤停复苏的原因;然而516例CVD事件中仅有7例事件是由心脏骤停复苏单一引起的,并且这也不太可能影响结果。最后,动脉粥样硬化检测是由其他公司代为检测的,因而并没有涵盖所有有亚临床症状的受试者。
综上所述,在基线时有亚临床症状的多种族人群中,Lp-PLA2质量和活性都与CVD、CHD风险有关。这里通过钙化的冠状动脉或劲动脉内中膜增厚判断有无亚临床疾病。无论基线时有无亚临床症状,患者增加的CVD风险是相近的。我们的研究中表明,Lp-PLA2与CVD似乎是通过某种与可检测的亚临床症状无关的机制相互关联的。
资金来源
本研究由合同N01-HC-95159,N01-HC-95160,N01-HC-95161,N01-HC-95162,N01-HC-95163,N01-HC-95164,N01-HC-95165,N01-HC-95166,N01-HC-95167,N01-HC-95168,N01-HC-95169,及国家心脏、肺和血液研究所K12-HL0837901拨款和国家研究中心UL1-TR-001079支持。同时也获得了葛兰素史克的研究者启动基金的支持。
披露
无
利益冲突
我们希望向以下与此项工作有关的人员披露:本项目统计学分析的部分支持来源于葛兰素史克给予McCelland博士的非限制性经济补助。葛兰素史克也资助了Lp-PLA2检测。Robert Rosenson曾为葛兰素史克咨询委员会一员。共同作者Mary Cushman和Nancy Jenny已从diaDexus公司获得了研究经费。
致谢
我们就其他研究者,工作人员和MESA研究的受试者做出的宝贵贡献表示感谢。MESA的所有受试者,研究者及组织机构列表见http://www.mesa-nhlbi.org.
参考文献(略)
作者:明德生物学术部


